美国FDA审批2023年批准的新药数量比2022年增加近50%
http://www.wenzhouzx.com 2024-01-03 19:59 来源 温州在线
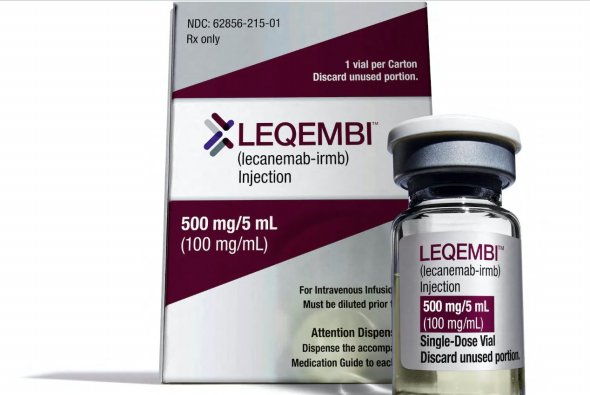
2023年1月20日获得的这张未注明日期的讲义图像中可以看到阿尔茨海默病药物LEQEMBI。
温州网讯,美国食品和药物管理局2023年批准的新药数量比2022年增加近50%,回到历史水平,分析师和投资者表示,这一改善可能会导致对生物技术公司的投资增加。
FDA认可的含有先前未批准的活性成分或分子的创新疗法,从2022年的37种和2021年的51种增加到2023年的55种。历史数据显示,FDA通常每年批准约45-50种新药,并达到2018年达到峰值59。
该机构批准了多种备受瞩目的疗法,例如礼来公司的肥胖药物Zepbound和卫材以及百健(Biogen)的阿尔茨海默病治疗药物Leqembi。除了55种新药之外,它还批准了5种基因疗法,包括VertexPharmaceuticals和CRISPRTherapeutics使用后者创新基因编辑技术的镰状细胞病治疗方法。
总部位于华盛顿的生命科学投资者集团Incubate的执行董事约翰·斯坦福(JohnStanley)表示:“很高兴看到FDA的批准数量增加。”他称基因编辑技术的进步尤其令人鼓舞。
他说:“我们的科学家可以做更多的事情,从这个角度来看,我们对即将发生的事情感到兴奋,不仅是在2024年,而且是在2024年之后。”
FDA在一份声明中表示,“批准的新药数量每年都有所不同,可能是由于多种因素造成的。”其中包括正在开发的新药的复杂性以及对疾病和疾病目标的科学认识的进步。
该机构没有提供2022年审批量大幅下降的具体原因。
TDCowen分析师RituBaral表示,COVID-19大流行可能是一个因素。当大流行来袭时,该机构从以创纪录的速度批准药品转向由远程工作人员操作,这造成了混乱和诸如影响药品审查的检查延迟等问题。
Baral说:“我们回到了峰值水平,这希望意味着工作流程中断、人员配备和带宽问题,以及最重要的是与开发人员的沟通有望得到改善。”她补充说,她预计FDA的批准水平将达到类似水平。2024年。
投资下降
过去两年对生物技术公司的投资只是历史水平的一小部分。
截至12月中旬,继2021年有108起首次公开募股(IPO)后,2022年和2023年各只有18起。据该券商称,PiperSandler追踪的一篮子生物技术基金在2023年出现了158亿美元的资本外流,这是自1992年以来最大的一次。
威廉·布莱尔(WilliamBlair)分析师在12月的一份报告中表示:“2023年是市场对能够获得资本的公司进行筛选的一年。”
他们指出,开发GLP-1减肥疗法的公司(与诺和诺德广受欢迎的Wegovy和礼来公司的Zepbound属于同一类)可以更好地进入IPO市场。
行业分析师还表示,投资者对高利率和政府对制药商审查的持续担忧可能会阻碍资金的全面复苏。
Jefferies分析师MichaelYee表示:“虽然我们预计资本市场不会回到2020-21年的峰值,但我们确实认为情况将会改善,窗口将会打开。”
Incubate的斯坦福表示,由于对该行业交易的监管力度加大、政府的药品价格谈判计划以及拜登政府威胁称,如果价格被认为低于预期,拜登政府将寻求没收由政府资助开发的药品专利,一些投资者可能仍保持观望。太高了。
本文“美国FDA批准新药”来源:http://www.wenzhouzx.com/jiankang/jcdd/84092.html,转载必须保留网址。编辑: yujeu
- 热门内容
- 网友热议
- 精彩内容

 同仁堂质量门 北京同
同仁堂质量门 北京同 拥有世界最大肱二头
拥有世界最大肱二头 浙江禽流感最新消息
浙江禽流感最新消息 江苏禽流感最新消息
江苏禽流感最新消息 大蒜的妙用 感冒吃大
大蒜的妙用 感冒吃大 h7n9诊疗方案 卫计委公
h7n9诊疗方案 卫计委公 美国FDA审批2023年批准
美国FDA审批2023年批准 拜耳因污染召回一批
拜耳因污染召回一批 卫材/渤健阿尔茨海默
卫材/渤健阿尔茨海默 美国FDA批准Ardelyx的肾
美国FDA批准Ardelyx的肾